Vacina contra Covid-19: Anvisa aprova uso emergencial do 2º lote da CoronaVac
Anvisa autorizou hoje, sexta-feira, 22 de janeiro (22/01), por unanimidade, o uso emergencial de mais 4,8 milhões de doses da CoronaVac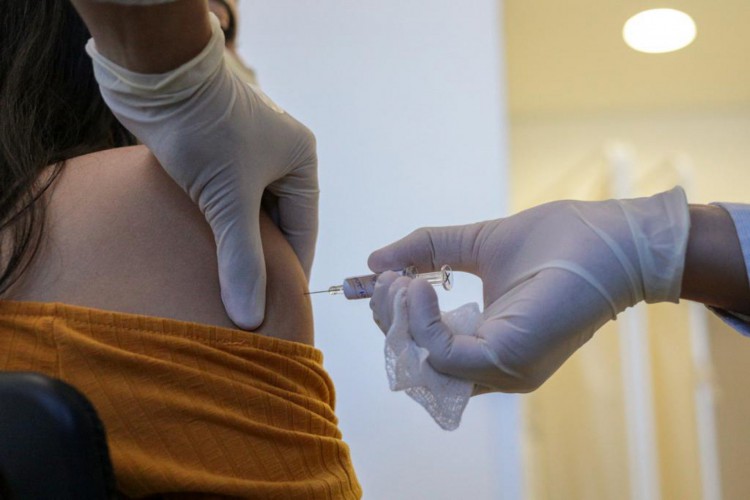
A diretoria colegiada da Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nesta sexta-feira, 22 de janeiro (22/01), por unanimidade, o uso emergencial de mais 4,8 milhões de doses da CoronaVac, desenvolvida em parceria entre a farmacêutica chinesa Sinovac e o Instituto Butantan, ligado ao governo de São Paulo.
A diferença da análise do segundo lote para o primeiro está no fato de que o envase e os processos de rotulagem e embalagem ocorrem no Instituto Butantan. Essas 4,8 milhões de doses são produzidas na China pela farmacêutica Sinovac, que envia para esses procedimentos na sede do centro de pesquisa paulista.
É + que streaming. É arte, cultura e história.
Como a Anvisa já havia aprovado no último domingo, 17, o primeiro lote importado da china, a avaliação da diretoria colegiada se deteve sobre as ações realizadas pelo Instituto Butantan.
A relatora, Meiruze Freitas, endossou os pareceres da área técnica e apresentou seu voto a favor da autorização, colocando alguns condicionantes sobre o acompanhamento de aplicação do imunizante para obter mais informações sobre sua estabilidade. "Mesmo em cenário de incerteza, uma vacina contra a covid-19 segura, capaz de prevenir e reduzir mortalidade e morbidade, pode ser autorizada para o uso emergencial, em especial pelo contexto desta pandemia, onde há poucos tratamentos de suporte disponíveis e não há medicamentos registrados na Anvisa com indicações específicas para o tratamento da covid-19”, concluiu.
As incertezas mencionadas pela relatora dizem respeito a determinados resultados que não foi possível confirmar no processo de análise. É o caso do prazo de validade da eficácia das doses, já que não houve tempo ainda para aferir isso.
A área técnica entendeu que na impossibilidade de ter tais informações, é necessário que o Instituto Butantan mantenha o monitoramento e o envio de dados à Anvisa, especialmente caso ocorra algum problema. Mas considerou que o benefício é mais efetivo do que essas incertezas e apontou que diante da velocidade da vacinação dificilmente as doses do lote analisado passariam da validade, estimada em 12 meses.
O diretor Rômison Mota seguiu a relatora, manifestando sua posição favorável à autorização uma vez que é possível concluir que “benefícios conhecidos e potenciais superam seus riscos conhecidos e potenciais”. O diretor Alex Campos foi o segundo a seguir o voto da relatora, fazendo menção aos alertas quanto ao cumprimento de monitoramento para avaliar as incertezas apontadas no relatório.
A diretora Cristiane Gomes foi na mesma linha. O presidente da Agência, Antônio Barra Torres, concluiu a votação também acompanhando a posição da diretora Meiruze Freitas e fechando a aprovação por unanimidade.
Quem produz a CoronaVac?
A CoronaVac é produzida no Brasil pelo Instituto Butantan, em São Paulo, em parceria com a empresa chinesa Sinovac. O acordo de produção foi do tipo "transferência de tecnologia", ou seja, a Sinovac desenvolveu o método para criação das vacinas, mas elas são feitas no Brasil.
A CoronaVac é segura?
Sim, a vacina é segura. Segundo Dimas Covas, diretor do Butantan, não houve efeitos colaterais graves nos mais de 9 mil voluntários que participaram dos testes. Ele chegou a afirmar que, dentre as quatro vacinas em teste no Brasil, a CoronaVac é a mais segura.
Nos testes, 35% dos voluntários tiveram reações leves, como dor no local da aplicação - que é feita por injeção intramuscular, no braço - ou dor de cabeça. Na China, onde mais de 50 mil voluntários foram testados, cerca de 5% tiveram efeitos colaterais, nenhum deles grave.
Além disso, a tecnologia usada para desenvolver a CoronaVac é utilizada há mais de 70 anos para criar diversos tipos de vacinas, como a da poliomielite e a da gripe. A técnica é considerada segura por órgãos de saúde no mundo inteiro, sendo a unica desvantagem o preço elevado das doses, porque é necessário cultivar o vírus para então inativá-lo.
A CoronaVac funciona? Qual a eficácia da vacina?
O Instituto Butantan anunciou hoje que a CoronaVac tem 78% de eficácia contra casos graves da doença e 100% contra casos leves e moderados. Isso significa que, entre os voluntários no teste da vacina, 78 a cada 100 estão imunes à doença, e o restante teve apenas casos leves ou assintomáticos de coronavírus.
O valor é considerado alto. Vacinas contra a gripe, por exemplo, atingem no máximo entre 50 e 60% de eficácia.
Como funciona a CoronaVac?
A CoronaVac usa a técnica de vírus inativado para proteger o organismo. No laboratório, os vírus são criados em um ambiente controlado, e em seguida passam por tratamentos químicos para impedi-los de se reproduzir. Ao serem injetados no paciente, os vírus não conseguem se replicar, e portanto não causam a doença. No entanto, o sistema imunológico reconhece o vírus inativado como uma ameaça como se fosse a versão "normal", e produz anticorpos para se defender. Com isso, no caso de uma contaminação real, o corpo já tem as defesas prontas para combater a infecção, e a doença não ocorre.
Por quanto tempo a CoronaVac protege o organismo?
A CoronaVac, assim como as outras vacinas contra o coronavírus, ainda não teve o período de eficácia determinado. O mesmo ocorre para quem teve Covid-19: ainda não se sabe por quanto tempo o paciente fica imune. Doenças como a gripe, por exemplo, precisam ter as vacinas atualizadas anualmente, pois o vírus sofre mutações conforme se prolifera na população, e vacinas antigas perdem a eficácia.
No caso do coronavírus, já se sabe que a reinfecção - quando a pessoa teve a doença, se curou, e foi novamente contaminada - é possível, especialmente em pacientes que apresentaram sintomas leves ou foram assintomáticos. Uma das hipóteses é que, nestas pessoas, a carga viral não foi alta o suficiente para gerar a chamada "memória imunológica". Situações como essa, apesar de raras, já foram confirmadas no Brasil.
Quando começará a vacinação com a CoronaVac?
Por enquanto há dois cronogramas planejados. Segundo o ministro da Saúde. Eduardo Pazuello, a vacinação poderia começar em 20 de janeiro caso a Agência Nacional de Vigilância Sanitária (Anvisa). No entanto, essa estimativa tem como base um estoque de outra vacina, a ChAdOx1 nCoV-19, desenvolvida pela AstraZeneca e pela Universidade de Oxford. Esta vacina tem 2 milhões de doses no Brasil em estoque: elas foram fabricadas pelo Instituto Serum, da Índia, maior produtor de vacinas do mundo, e importadas pelo governo. A Fundação Oswaldo Cruz (Fiocruz) deve começar a produção nacional desta vacina também no final deste mês.
Para a vacinação com a CoronaVac especificamente, a estimativa é que ela comece em 25 de janeiro, capitaneada pelo governo do estado de São Paulo. O cronograma inicial do governo paulista visa atender a grupos de risco e tem as seguintes datas:
25 de janeiro - Trabalhadores da saúde, indígenas e quilombolas
8 de fevereiro - 75 anos ou mais
15 de fevereiro - 70 a 74 anos
22 de fevereiro - 65 a 69 anos
1º de março - 60 a 64 anos
Quantas doses serão feitas da CoronaVac?
O contrato de compra anunciado hoje pelo Ministério da Saúde prevê um total de 100 milhões de doses da CoronaVac para 2021, com uma aquisição inicial de 46 milhões de doses e possibilidade de renovação para mais 54 milhões, totalizando os 100 milhões.
Ao todo, é estimado pelo Ministério que sejam aplicadas 354 milhões de doses da vacina contra o coronavírus no Brasil em 2021. Além das 100 milhões de doses de CoronaVac e das 2 milhões já importadas da Índia, cerca de 210 milhões da ChAdOx1 nCoV-19 seriam fabricadas pela Fiocruz, e mais 42,5 milhões serão adquiridas pelo acordo internacional Covax Facility. Com esta quantidade, seria possível vacinar cerca de 177 milhões de pessoas, ou 84% da população brasileira, pois cada vacina demanda duas doses para atingir a maior eficácia.
As compras foram possibilitadas por Medida Provisória (MP) assinada nessa terça-feira, 6, pelo presidente da República, Jair Bolsonaro (sem partido). A MP permite a compra de vacinas antes mesmo da aprovação pela Anvisa, ao contrário do que ocorria antes, que exigia registro da agência para a negociação.
Além das 354 milhões de doses, ainda há negociação do governo com a Pfizer, e testes no Brasil de vacinas produzidas pela Janssen. A empresa farmacêutica União Química solicitou aprovação da Anvisa para estudos com a Sputnik V, fabricada em parceria com o Centro Gamaleïa, da Rússia. Para estas três alternativas, no entanto, não há previsão de data para aplicação no Brasil ou quantas doses de cada estariam disponíveis.
A CoronaVac será usada em outros países?
Sim. Além do Brasil, a própria China, onde a vacina foi desenvolvida, já está aplicando de forma emergencial em profissionais de saúde e funcionários públicos. A Indonésia e a Turquia fecharam, cada uma, contratos para compra de 50 milhões de doses da CoronaVac, e o Chile tem um acordo para adquirir 20 milhões.
Quem vai poder tomar a CoronaVac?
Em um primeiro momento, a vacinação será direcionada a determinados grupos de risco - indígenas, quilombolas, profissionais de saúde e pessoas idosas. A intenção é reduzir o risco para quem tem exposição constante ao coronavírus, no caso de quem trabalha na área médica, e atender a categorias com as maiores taxas de mortalidade, nos outros grupos. Somente após esta etapa a vacinação será oferecida à população geral.
Todavia, devido ao processo emergencial para desenvolver e aprovar as vacinas, não foram realizados estudos para determinar a segurança da imunização em gestantes e pessoas menores de 18 anos, segundo o próprio Butantan. Estes dois grupos, portanto, não poderão se vacinar com a CoronaVac por enquanto.
Com Agência Brasil
Dúvidas, Críticas e Sugestões? Fale com a gente
