Anvisa discute mudanças no marco regulatório dos laboratórios de análises clínicas
Agência promoveu audiência pública nesta terça-feira, 26, para debater um novo modelo regulatório para o setor. Encontro teve a participação de pesquisadores, especialistas e representantes da sociedade civil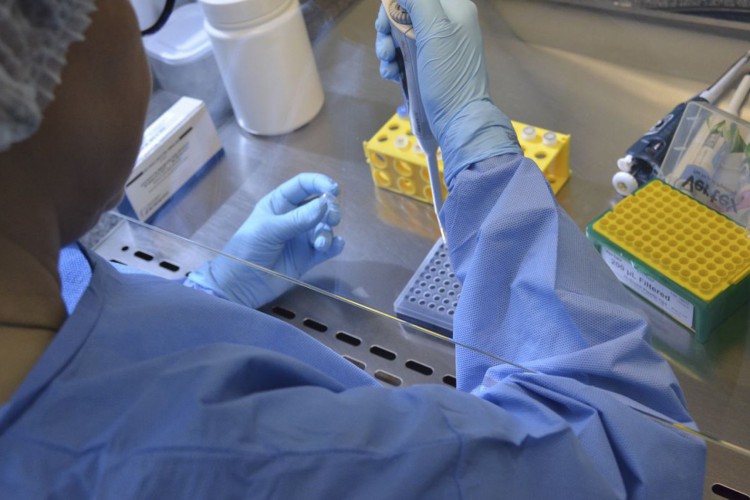
A Agência Nacional de Vigilância Sanitária (Anvisa) iniciou uma série de discussões sobre possíveis mudanças no marco regulatório que estabelece as normas de funcionamento de laboratórios de análises clínicas e estabelecimentos de saúde prestadores de serviços de apoio diagnóstico e terapêutico. A primeira fase da transição tem como base a participação social. Por isso, nesta terça-feira, 26, o órgão promoveu uma audiência pública com especialistas, pesquisadores e representantes da sociedade civil para tratar sobre o tema.
O encontro foi convocado pela Diretoria Colegiada da Agência. De acordo com a diretora Cristiane Rose Gomes, relatora e supervisora da matéria, a audiência é um passo importante para a construção do novo modelo regulatório do setor.
É + que streaming. É arte, cultura e história.
“Nosso intuito é construir um marco normativo claro e efetivo ao controle sanitário desses serviços, cujos impactos de sua implementação sejam mapeados e coadunem com os objetivos regulatórios inicialmente propostos", ressaltou.
A diretora ainda acrescentou que, com os avanços tecnológicos registrados nos últimos anos no setor de análises clínicas, cabe à Agência avaliar os requisitos indispensáveis para o funcionamento de novas ferramentas, de modo a garantir que os serviços sejam prestados de forma eficaz e segura.
"Procuramos ponderar situações trazidas pela evolução da tecnologia sem perder nossa responsabilidade de prover uma norma de eficácia, segurança e qualidade para um mercado cujo protagonismo na assistência à saúde é indubitável”, ponderou Cristiane.
De acordo com a Anvisa, a revisão nas regras atuais é motivada, principalmente, pela necessidade de aprimoramento dos parâmetros de qualidade e de adequação do instrumento regulatório frente à evolução tecnológica do setor, além da questão da ampliação do acesso aos testes clínicos.
“Precisamos pensar na ampliação do acesso a esses procedimentos de maneira segura, considerando os riscos sanitários inerentes às etapas do processo com foco na qualidade do produto e do serviço oferecidos e na segurança do paciente”, defendeu a gerente-geral de tecnologia em serviços da Anvisa, Renata Hurtado. Ela explica que, a partir da audiência, a equipe técnica da Agência analisará as contribuições recebidas e o compilado será analisado pela diretoria relatora do processo.
A possível alteração normativa do setor também foi tema de uma consulta pública lançada pela Anvisa em setembro de 2020. Em apenas dois dias, foram registradas 2.965 contribuições.
Também foram realizadas consultas internas dirigidas a vigilâncias sanitárias estaduais e municipais. Segundo a Agência, os procedimentos são fundamentais para que sejam avaliados os impactos de uma eventual regulamentação. As próximas etapas do processo devem ser anunciadas em breve.
OUÇA O PODCAST VOO 168 BASTIDORES

