Anvisa recebe pedido de registro definitivo da vacina da Pfizer
Caso aprovado, a vacina poderá ser comercializada, distribuída e utilizada pela população de acordo com os termos estabelecidos pela bula do imunizante. Esse é o segundo pedido de registro definitivo, o primeiro foi da Fiocruz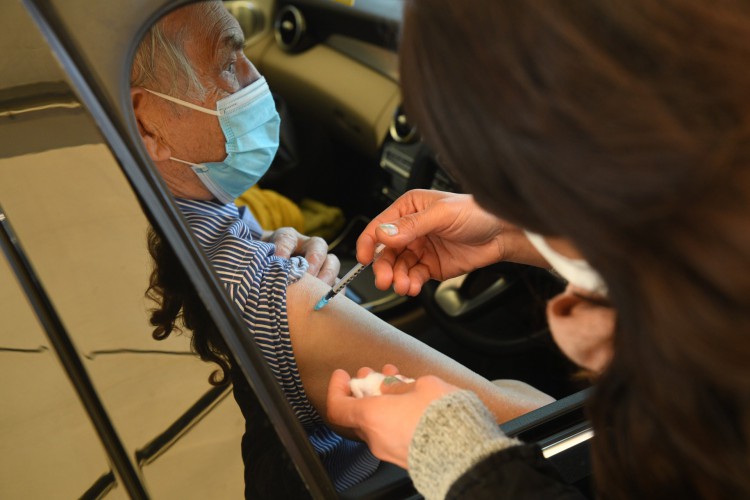
O laboratório americano Pfizer fez pedido para registro definitivo da vacina contra Covid-19 na manhã deste sábado, 6. Enviado à Agência Nacional de Vigilância Sanitária (Anvisa), o pedido tem até 60 dias para ser analisado. Este é o segundo pedido de registro definitivo encaminhado ao órgão, o primeiro foi feito no dia 29 de janeiro pela Fundação Oswaldo Cruz (Fiocruz) para a vacina da universidade de Oxford.
Caso aprovado pela agência reguladora, o registro é sinal verde para que a vacina seja comercializada, distribuída e utilizada pela população, nos termos estabelecidos pela bula. “O registro é a avaliação completa com dados mais robustos dos estudos de qualidade, eficácia e segurança, bem como do plano de mitigação dos riscos e da adoção das medidas de monitoramento”, informou a Anvisa em comunicado.
Seja assinante O POVO+
Tenha acesso a todos os conteúdos exclusivos, colunistas, acessos ilimitados e descontos em lojas, farmácias e muito mais.
AssineLeia Também | Médico descontextualiza manual da Pfizer para sugerir alterações genéticas pela vacina
+ Covax enviará vacinas de AstraZeneca e Pfizer à América Latina
+ Vacina da Pfizer causaria frustração nos brasileiros, diz ministério
“O pedido de registro da vacina junto à Anvisa é a etapa final do processo de submissão contínua estabelecido pela agência para acelerar os registros de vacinas contra a covid-19. A companhia continuará trabalhando junto com a Anvisa para que o processo transcorra da melhor maneira possível, sempre pautadospor critérios técnicos e científicos”, disse neste sábado, Márjori Dulcine, diretora médica da Pfizer Brasil, de acordo com a assessoria de imprensa da farmacêutica.
Segundo a Pfizer, 2,9 mil voluntários participaram dos testes clínicos de sua vacina no Brasil. No mundo todo, foram 44 mil participantes em 150 centros de seis países, incluindo África do Sul, Alemanha, Argentina, Estados Unidos e Turquia. Resultados da terceira e última fase de testes do imunizante, divulgados em novembro, apontaram eficácia de 95% contra o novo coronavírus.
O registro dos imunizantes deve obedecer regras estabelecidas pela Anvisa, para garantir que as vacinas sejam seguras e adequadas para imunizar e não causar dano à população brasileira. O órgão ressaltou que não tem intenção de “impor barreiras ou dificuldades” para a finalização do processo, mas sim garantir os critérios definidos.
Cristiano Zerbini, coordenador dos testes da vacina no Brasil, disse que a apresentação do pedido é mais um passo para que se tenha os imunizantes disponíveis para todos os brasileiros. “É uma vacina excelente, estou torcendo para que haja um acordo entre o Ministério da Saúde e a Pfizer”, disse à CNN.
